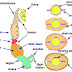
Bệnh Dịch Tả Trâu Bò (Pestis Bovium, Rinderpest)
 |
| Dịch tả trên trâu, bò. Ảnh minh họa |
Vào thế kỷ 18 và 19, nhiều ổ dịch lớn dịch tả trâu bò đã gây chết hàng triệu con trâu bò ở Châu Âu. Vào những năm 1930, trừ một phần Thổ Nhĩ Kỳ, châu Au không còn bệnh và từ đó đến nay chỉ có những ổ lẻ tẻ xảy ra. Tuy nhiên bệnh vẫn tiếp tục tồn tại ở châu Á nhất là ở Ấn Độ, Bangladesh, Nepal. Năm 1982-1983 thấy có bệnh ở vùng Trung Đông. Bệnh đưa vào châu Phi từ đầu thể kỷ 19 và gây các trận đại dịch trong các năm từ 1889-1897. Đến nay châu Phi vẫn còn bệnh, mặc dù có các kế hoạch tiêm phòng liên quốc gia trong các năm từ 1962-1975, nhưng vẫn còn dịch xảy ra thường xuyên trong vùng này (Scott,1985). Ở Việt Nam từ những năm 1960 đã không còn thấy bệnh xuất hiện.
1. Căn bệnh:
Virus gây bệnh dịch tả trâu bò thuộc họ Paramyxoviridae, giống Morbillivirus. Các loài khác trong giống Morbillivirus là virus sởi (measles), bệnh chó non (distemper) và virus bệnh dịch tả dê cừu (PPR: peste des petits ruminants) có liên hệ nhau về kháng nguyên. Các Morbillivirus có hình dạng thay đổi, có envelop, kích thước thay đổi 150-300 nm và chứa một chuỗi RNA không phân đoạn. Bộ gen này mã hóa cho 6 loại protein cấu trúc và một protein không cấu trúc. Các protein cấu trúc của virus gồm có protein của nucleocapsid (gọi tắt là N) bao quanh chuỗi RNA, một phân tử polymerase lớn (L), một phân tử polymerase nhỏ (P), protein của matrix (M) liên kết với envelop và hai glycoprotein của envelop: H (hemagglutinin) và F (Fusion). Gen P cho thấy đồng nhất giữa các loài trong giống Morbillivirus (Barrett và Underwood, 1985).
 |
| Cấu trúc virus giống Morbillivirus |
Chỉ có một serotyp duy nhất và virus dịch tả trâu bò có thể phân biệt với virus PPR bằng phản ứng trung hòa chéo. Hiện nay không thể phân biệt 2 bệnh bằng huyết thanh của thú khỏi bệnh. Tuy nhiên chúng có thể phân biệt bằng cách so sánh các protein trên polyacrylamide do protein N có trọng lượng phân tử khác nhau (Diallo và ctv, 1987). Ngoài ra có thể phân biệt 2 virus bằng cách cho lai chéo với các đoạn mồi c. DNA (Diallo và ctv, 1989).
Virus mẫn cảm với các dung môi hòa tan lipid, tương đối mẫn cảm với nhiệt và không bền ở pH thấp. Nó cũng dễ bị diệt khi phơi ra ánh sáng và bị diệt khi ẩm độ tương đối ở khoảng 40-60% RH. Độc lực mất đi khi ở trong glycerol hoặc nước, ngược lại bền ở dung dịch 0,85% NaCl và nhiệt độ thấp. Magnesium sulphat làm gia tăng tính chịu nhiệt của virus.
2. Các loài thú mẫn cảm:
Bệnh dịch tả trâu bò có thể gây ra trên các thú thuộc bộ Artiodactyla (Scott, 1964), đặc biệt là họ Bovidae, Suidae và Cervidae (Plowright, 1968). Trong số đó thì trâu bò, trâu caffer (Syncerus caffer) và con yak là mẫn cảm nhất. Bệnh xảy ra trên dê, cừu cũng như ở heo được thấy ở An Độ. Ngoài ra bệnh có thể gặp ở lạc đà (nhẹ). Một số loài động vật hoang dã cũng mắc bệnh; Taurotragus oryx (bò rừng), Kudu (Tragelaphus imberis), hươu cao cổ (Giraffa camelopardis) và heo rừng ( Phacochoerus aethiopicus).
3. Truyền lây:
Bệnh có thể lây do trực tiếp tiếp xúc giữa thú bệnh và thú mẫn cảm, do hít phải các hạt aerosol có virus hoặc ăn phải các chất tiết. Những trường hợp lây lan do tiếp xúc gián tiếp thì hiếm hơn, qua chất độn chuồng hoặc nước. Heo mắc bệnh khi ăn thịt các quày thịt bệnh. Các dòng virus thì khác nhau về độc lực và khả năng gây bệnh tùy theo loài gia súc.
4. Sinh bệnh học:
Cảm nhiễm qua đường hô hấp trên với các virus nhân lên đầu tiên ở hạch hạnh nhân và hạch lâm ba gần đó (Plowright, 1968), virus xâm nhập vào máu chủ yếu trên đại thực bào để đến các mô lâm ba và màng niêm của đường tiêu hóa và hô hấp. Thời kỳ ủ bệnh kéo dài từ 2 đến 9 ngày trước khi xuất hiện triệu chứng sốt. Giai đoạn tiền chứng (prodromal period) khoảng 2-5 ngày. Virus được bài xuất trong các chất tiết, đỉnh cao sinh sản của virus nằm trong khoảng thời gian sốt của thời kỳ tiền chứng nhưng kéo dài đến sau khi xuất hiện các bệnh tích loét. Hàm lượng virus giảm xuống khi kháng thể được tạo ra và viremia ngưng trước khi virus biến mất khỏi mô bào vào ngày 14 sau khi bắt đầu sốt. Ơ một số dòng virus, viremia có thể xảy ra từ 4-6 ngày mà không thể hiện các bệnh tích (độc lực thấp).
5. triệu chứng lâm sàng:
Các triệu chứng của bệnh trên trâu bò và các ký chủ tự nhiên khác thường giống nhau nhưng mức trầm trọng thay đổi rất nhiều tùy thuộc vào chủng virus và sức đề kháng của thú (tự nhiên hay tiếp thu).
Bệnh có thể ở thể quá cấp, cấp, bán cấp hoặc mãn tính (Plowright, 1968).
Thể bệnh cấp tính điển hình có thể chia làm 4 giai đoạn hay thời kỳ : ủ bệnh, tiền chứng, giai đoạn niêm mạc (giai đoạn loét) và hồi phục.
Thời kỳ ủ bệnh:( xem ở trên ) 2-9 ngày.
Thời kỳ tiền chứng: có đặc điểm là xuất hiện sốt thình lình, tăng dần đến đỉnh cao vào ngày thứ 2 hoặc thứ 3 kể từ lúc bắt đầu sốt. Triệu chứng còn có uể oải hoặc nằm một chỗ, mất tính thèm ăn và giảm sản xuất sữa (bò cái). Các niêm mạc bị sung huyết, gương mũi khô và bắt đầu có chất tiết lỏng chảy ra ở mắt và mũi. Nhịp tim đập không đều (tachycardia), tần số hô hấp tăng, ngừng nhai lại và táo bón. Thời kỳ này kéo dài khoảng 3 ngày và các bệnh tích xuất hiện 2-5 ngày sau khi bắt đầu sốt.
Thời kỳ niêm mạc (loét): các bệnh tích đầu tiên là các đốm hoại tử nhỏ cùng xuất huyết các mao mạch trên bề mặt niêm mạc miệng, đặc biệt ở nướu răng hàm dưới và đầu các gai thịt trong miệng. Hoại tử có thể lan đến môi, nướu răng hàm trên, khẩu cái cứng và mặt bụng của lưỡi. Bệnh tích tương tự cũng thấy ở niêm mạc mũi, âm hộ và bao quy đầu có thể sớm hơn ở miệng. Các bệnh tích có thể hợp lại tạo thành các mảng hoại tử có mùi rất khó ngửi. Nước bọt cũng tiết rất nhiều và trong giai đoạn này các chất tiết ở mắt và mũi ngày càng nhiều và giống như có mủ.
Thú trong giai đoạn này rất mệt mõi và thở khó khăn, nhưng ít khi có viêm phổi. Tiêu chảy thường xuất hiện giữa ngày thứ 4 và ngày thứ 7 trong giai đoạn sốt và 1-2 ngày sau khi xuất hiện các vết loét. Đầu tiên thú đi phân rất lỏng, sau đó đi kiết và có thể có các mảnh niêm mạc ruột. Thú mất nước nhanh chóng nên rất yếu ớt, nằm một chỗ và chết trong vòng 6-12 ngày kể từ khi có sốt. Tỷ lệ chết bệnh hơn 90% khi thú mẫn cảm tiếp xúc với chủng virus cường độc.
Thể bệnh nhẹ (bán cấp) có thể gặp trên thú có miễn dịch phần nào hoặc mắc bệnh do chủng virus ít độc sẽ có các triệu chứng chung nhẹ hơn và bệnh tích loét ở niêm mạc ít lan tràn hơn. Sốt có thể hơi giảm vào giữa giai đoạn loét và sau 1-2 ngày có thể trở lại thân nhiệt bình thường. Lúc bấy giờ tiêu chảy ngừng, bệnh tích ở miệng giảm nhanh. Ngoài ra cũng có những trường hợp chỉ thấy tiêu chảy thoáng qua. Nhưng dù ở thể bệnh nào thì cũng có thể phát hiện kháng nguyên virus trong chất tiết mắt (Anderson, 1990).
Thời kỳ hồi phục: Các bệnh tích trong miệng có thể lành sau khi xuất hiện 3-5 ngày. Tiêu chảy có thể kéo dài lâu hơn. Sự bình phục hoàn toàn ở thể cấp tính cần khoảng 4 tuần lễ phụ thuộc vào điều kiện ngoại cảnh và chế độ dinh dưỡng.
6. bệnh tích:
6.1 Bệnh tích đại thể:
Bệnh tích kinh điển cho thấy quày thịt mất nước. Gầy ốm, dính đất và hôi thối. Mũi và má có các chất dịch đặc như mủ, mí mắt sụp và kết mạc sung huyết. Trong xoang miệng, thường có sự tróc rất nhiều biểu bì bị hoại tử, phân biệt rất rõ với vùng niêm mạc không bệnh tích. Các bệnh tích thường lan rộng đến khẩu cái mềm và có thể đến hầu và phần trên thực quản. Dạ cỏ, tổ ong, lá sách thường không bị ảnh hưởng mặc dù đôi khi thấy các đốm hoại tử ở các gai của dạ cỏ. Dạ dầy thật (abomasum) bị nặng nhất, đặc biệt vùng hạ vị, cho thấy sung huyết nặng, xuất huyết lấm tấm và phù thũng ở lớp dưới màng niêm (submucosa). Hoại tử ở lớp thượng bì tạo cho niêm mạc có màu xám đen. Ruột non thường không bệnh tích ngoại trừ các biến đổi rõ nét ở các nốt Peyer bị hoại tử nang lympho và tróc ra tạo các bệnh tích tròn sung huyết hoặc xám đen lại. Ơ ruột già, các biến đổi gặp ở van hồi-manh và dọc theo các nếp gấp ở niêm mạc manh tràng, trực tràng, ruột già. Các nếp này có vẻ rất sung huyết trong các trường hợp chết cấp tính hoặc chuyển sang màu đen sạm trong các trường hợp bệnh kéo dài hơn, một số nơi gọi là các vạch như ngựa vằn. Các mụn loét cũng có thể gặp ở đường sinh dục hoặc tiết niệu.
6.2 Bệnh tích vi thể:
Virus có khuynh hướng thích các tế bào lympho tạo ra các nốt hoại tử ở các trung tâm mầm và sự xuất hiện các tế bào khổng lồ có nhiều nhân (hợp bào) vào khoảng 8 ngày sau khi cảm nhiễm. Các thể bao hàm trong tế bào chất và trong nhân tế bào đã được mô tả (Plowright, 1968). Các biểu bì vẩy, nhất là ở phần trên đường tiêu hóa cho thấy tạo thành hợp bào, cùng các biến đổi thoái hóa, tiếp đó hoại tử và tróc ra để tạo thành các nốt loét.
7. chẩn đoán:
Xác định căn bệnh trong phòng thí nghiệm chủ yếu dựa trên sự chứng tỏ kháng nguyên kết tủa hiện diện ở lách, hạch lâm ba hoặc chất tiết ở mắt, mũi trên con vật bệnh thể cấp tính. Đồng thời có thể phân lập virus. Còn có thể chẩn đoán bằng cách phát hiện kháng thể đặc hiệu từ thú đã bị bệnh (Scott và ctv, 1986).
7.1 Phân lập virus:
Phân lập virus dịch tả trâu bò từ máu cần chú ý dùng các chất kháng đông như heparin (10 UI/ml) hoặc EDTA (0,5 mg/ml). Mẫu còn có thể gồm hạch (hạch trước vai hoặc hạch ruột), lách. Bệnh phẩm được bảo quản trong nước đá khi vận chuyển nhưng không nên dùng glycerol vì làm bất hoạt virus.
Các kháng nguyên kết tủa có thể có trong chất tiết ở mắt thú bệnh trong giai đoạn tiền chứng hoặc loét. Chúng được lấy bằng cách dùng que bông quét vào giữa 2 mí mắt. Huyết thanh vạch vô trùng có thể được lấy mẫu từ các thú đã được đánh số trong giai đoạn cấp tính của bệnh và lần sau vào lúc 2 tuần sau khi giảm bệnh. Các mẫu huyết thanh bắt cặp (paired serum) được dùng để kiểm tra sự gia tăng lượng kháng thể trung hòa.
Máu đã chống đông được ly tâm 2500 vòng/phút trong 10 phút để tạo ra một lớp đệm ở giữa phần huyết tương và hồng cầu. Nó được lấy ra một cách vô trùng rồi trộn với 20 ml nước muối sinh lý và được ly tâm lại như trong phương pháp rửa để tách mọi kháng thể trung hòa xuất hiện sớm trong huyết tương. Các tế bào còn lại được pha thành huyễn dịch và cho 2 ml vào mỗi ống tế bào thận bê hoặc tế bào Vero. Các ống nghiệm có tế bào này được kiểm tra định kỳ dưới kính hiển vi để phát hiện tác động gây bệnh tích tế bào như tế bào bị tròn, co lại với các cầu nối tế bào chất bị kéo dài ra, hoặc tạo tế bào khổng lồ. Phân lập virus có thể xác định nhờ chứng tỏ kháng nguyên gây kết tủa (precipitin) trong mảnh xác tế bào hoặc bằng miễn dịch men (immunoperoxidase) tạo màu, hoặc phản ứng trung hòa với kháng huyết thanh đặc hiệu.
Người ta có thể dùng huyễn dịch 10% (w/v) của hạch lâm ba hoặc lách để phân lập virus thay vì như ở trên, bằng cách dầm mô hạch lâm ba trong môi trường không có huyết thanh.
7.2 Phát hiện kháng nguyên virus:
* Test miễn dịch khuếch tán (AGID) có thể thực hiện trên các đĩa Petri nhựa hoặc trên các phiến lame. Bề mặt phải được phủ một lớp agar dầy độ 4 mm (dung dịch lỏng 1% agar hoặc agarose). Các lỗ thường được sắp xếp kiểu lục giác với 6 lỗ chung quanh và 1 lỗ ở giữa. Trên phiến kính, các lỗ có đường kính 3 mm và cách nhau 2 mm. Trên đĩa Petri, đường kính có thể 4 mm và khoảng cách giữa các lỗ độ 3 mm. Các lỗ càng để gần nhau thì thời gian cần cho phản ứng càng ngắn. Tốt nhất thực hiện ở 4 0C hoặc nhiệt độ môi trường thấp. Dùng một pipette Pasteur, huyết thanh tối miễn dịch chống dịch tả trâu bò (chế từ thỏ) được cho vào lỗ ở trung tâm. Tương tự đối chứng kháng nguyên dương thu nhận từ môi trường tế bào nuôi cấy virus dịch tả trâu bò hoặc từ hạch lympho màng treo ruột (của thú bị gây bệnh bằng virus) cho vào các lỗ chung quanh: 1, 3 và 5. Kháng nguyên đối chứng âm được cho vào lỗ số 4. Kháng nguyên cần chẩn đoán dùng cho phản ứng này có thể lấy từ dịch ở mặt cắt lách hoặc hạch lâm ba. Nếu không có chất dịch trên, có thể lấy một mẫu bệnh phẩm nhỏ (hạch, lách) nghiền với cát và một ít nước muối sinh lý. Dịch tiết ở mắt được lấy trực tiếp nhờ một que bông. Các mẫu bệnh phẩm được cho vào lỗ số 2 và 6. Đánh giá kết quả sau 2 giờ sẽ thấy xuất hiện các đường kết tủa. Kết quả chỉ được công nhận khi có đường kết tủa xảy ra tương ứng với kháng nguyên đối chứng dương.
* Test miễn dịch điện di đối lưu ( CIE ) có thể cho kết quả dương tính cao hơn một chút so với AGID. Phản ứng thực hiện trên các phiến lame phủ một lớp agar 1% dầy 2 mm (hoặc agarose 0,025% trong đệm veronal-acetat pH 8,6). Các lỗ được chia thành từng cặp bởi các đường cắt cách chúng độ 6 mm, phía bên trái là anod cho kháng huyết thanh chống dịch tả trâu bò, phía bên catod cho vào đầy mẫu bệnh phẩm hoặc kháng nguyên đối chứng dương, kháng nguyên đối chứng âm. Mẫu được cho chạy điện 40-60 phút với dòng điện không đổi 10 mA/phiến kính, sau đó đánh giá kết quả kết tủa.
Nhiều phương pháp khác nhau cũng có thể ứng dụng để tìm kháng nguyên virus dịch tả trâu bò, trong đó biện pháp phổ biến nhất hiện nay là test immunoperoxidase trực tiếp và gián tiếp.
Cẩn thận đối với các trường hợp khó thấy triệu chứng lâm sàng hoặc các test phát hiện kháng nguyên của group (nhóm) không rõ ràng phân biệt giữa dịch tả trâu bò và dịch tả dê cừu khi chúng đều gây bệnh cho cừu và dê. Người ta có thể dùng các đoạn mồi (probe) cDNA đặc hiệu cho RNA thông tin của protein capsid ở mỗi virus.
7.3 Phản ứng huyết thanh học (serological tests) phát hiện kháng thể:
7.3.1 Trung hòa virus (VN):
Phản ứng trung hòa virus được thực hiện trên môi trường tế bào thận bê hoặc Vero, nuôi trong các ống được xoay tròn. Huyết thanh làm bất hoạt được pha loãng 1:2 hoặc 1:10 và trộn với một huyễn dịch virus tiêu chuẩn chứa khoảng 103 TCID50/ml. Hỗn hợp virus và huyết thanh với thể tích bằng nhau được giữ qua đêm ở 4 0C . Sau đó chuyển hỗn hợp vào mỗi ống nghiệm (5 ống, mỗi ống cho vào 0,2ml), cho thêm vào mỗi ống 1 ml huyễn dịch tế bào (2 x105/ml). các ống được đặt nghiêng 3 ngày ở 370C. Những ống nào có virus phát triển (gây bệnh tích tế bào ) sẽ bị loại. Môi trường sẽ được thay mới và các tube cho quay tròn để rồi quan sát đánh giá kết quả vào ngày thứ 7. Để tính toán, lượng virus dùng trong phản ứng được coi như thích hợp nếu nằm trong khoảng 101,8-102,9 TCID50/ống. Các độ pha loãng của huyết thanh được coi như loãng gấp đôi sau khi trộn với dịch virus. Bất cứ mức kháng thể nào được phát hiện, ngay cả ở 1:2 cũng được coi là dương tính. Tuy nhiên, để đánh giá miễn dịch sau khi tiêm vaccin thì độ pha loãng 1:8 được coi như mức khởi đầu.
Phản ứng trung hòa virus trong các vỉ nhỏ cũng được thực hiện. Các vỉ có lỗ đáy bằng chứa tế bào nuôi cấy (98 lỗ giếng, huyết thanh được pha loãng 1:2 theo dãy giảm dần với micropipette (25 l / lỗ). Sau đó cho thêm 25 l huyễn dịch virus dịch tả trâu bò với nồng độ 100 TCID50/lỗ. U qua đêm ở 4 0C, cho thêm 100l tế bào thận bê hoặc Vero với lượng 1x103,6/ml cho mỗi lỗ. Các vỉ nhựa được dán băng keo, ủ ở 370C và được đánh giá kết quả qua kính hiển vi sau 7 ngày trở lên. Tiêu chuẩn của mức chấp nhận cũng tương tự đã trên.
Test này có thể dùng kiểm tra huyết thanh của trâu bò sau khi chủng vaccin. Tuy nhiên, không dùng để chẩn đoán huyết thanh dê, cừu do sự hiện diện của các tác nhân gây cản trở virus không đặc hiệu trong huyết thanh.
7.3.2 Phản ứng ELISA gián tiếp:
Để kiểm tra đại trà các huyết thanh trâu bò sau tiêm phòng vaccin, người ta đã phát minh test ELISA gián tiếp với pha rắn. Kháng nguyên được chế từ các tế bào nhiễm chủng virus vaccin RBOK nuôi trong môi trường không có serum và có thể được dùng pha loãng với nước muối đệm phosphat (PBS) thành huyễn dịch 1:100. Sự gắn xảy ra ở 370C trong 60 phút dùng một máy lắc quay tròn, kế đó rửa và làm khô. Các mẫu huyết thanh (cần kiểm tra ) được pha loãng theo dãy 1:2 với lượng 60 l bằng cách pha 15 l serum với 45 l dung dịch đệm (dùng loại mới pha), trong đó chứa 100 l Tween 20 (0,1%) và 5 gr sữa không kem (bột) cho mỗi 100 ml PBS. Bước pha loãng này có thể thực hiện trong các lỗ giếng. Vỉ nhựa trên được ủ tiếp ở 370C trong 60 phút rồi rửa đi. Kháng thể kết hợp (bám) được phát hiện bằng kháng kháng thể IgG bò chế từ thỏ có gắn enzym peroxidase được pha sẵn ở nồng độ khoảng 1:10 000, tiếp đó là rửa rồi thêm OPD (orthophenyl diamine) làm cơ chất. Phản ứng được cho ngừng bằng cách cho thêm acid sulfuric hoặc trichloroacetic acid và đo với máy đọc ELISA ở bước sóng 492 nm.
7.3.3. ELISA cạnh tranh:
Phản ứng ELISA cạnh tranh dựa trên sự tranh gắn vào kháng nguyên dịch tả trâu bò (gắn sẵn trên pha rắn giữa kháng thể đơn dòng đặc hiệu dịch tả trâu bò và kháng thể trong mẫu huyết thanh cần kiểm tra. Sự có mặt kháng thể chống virus dịch tả trâu bò trong mẫu huyết thanh sẽ phong bế sự kết hợp kháng nguyên với kháng thể đơn dòng, gây ra sự giảm tạo màu sau khi thêm conjugate có gắn enzym và cơ chất. Vì đây là test thực hiện trên pha rắn, các bước rửa phải thực hiện sau mỗi bước để bảo đảm loại ra các chất không phản ứng.
Kháng nguyên cho phản ứng ELISA được chuẩn bị từ môi trường nuôi cấy tế bào thận bê (Madin Darby) nuôi cấy virus vaccin Kabete“O” (nhược độc). Kháng nguyên được sản xuất bằng cách cho kết tủa với ammonium sulfate hoặc bằng cách phối hợp xử lý bằng siêu âm và ly tâm. Kháng thể đơn dòng chuyên biệt cho dịch tả trâu bò (không cho phản ứng với virus dịch tả dê cừu (PPR). Đệm PBS pH 7,6 dùng pha kháng nguyên và các thuốc thử khác được thêm vào 0,1% (v/v) chất tẩy Tween 20 và 0,3% (v/v) huyết thanh bò khỏe mạnh (đệm dùng phong bế). Các thể tích 50 l được dùng thống nhất nhau và các giai đoạn được ủ ở 370C 1 giờ trên máy lắc xoay tròn.
Các vỉ được phủ kháng nguyên ở nồng độ thích hợp đã định trước (thường là 1:100) trong PBS, và sau khi ủ các vỉ được rửa 3 lần trong PBS pha loãng 1:5 (dung dịch rửa) để loại bỏ các kháng nguyên không gắn vào vỉ. Huyết thanh cần chẩn đoán được cho vào bằng cách pha loãng 10 l serum nguyên với 40 l dung dịch đệm. Các đối chứng dương tính rõ, dương tính yếu và âm tính của huyết thanh cũng được cho vào các vỉ. Sau đó cho thêm 50 l kháng thể đơn dòng ở độ pha loãng định trước (thường là 1:100) trong dung dịch đệm. Sau đó là ủ và rửa, người ta lại cho thêm vào 50 l conjugate kháng Ig chuột chế từ thỏ gắn peroxidase ở nồng độ định trước (thường là 1:100). Sau khi ủ lần chót, các vỉ được rửa và 50 l cơ chất / chất hiện màu (H2O2/ orthophenylene diamine) được cho vào và phản ứng được để xảy ra trong 10 phút. Màu tạo ra được ngưng khi cho thêm acid sulfuric 1M và kết quả được đọc ở máy đọc ELISA có độ dài sóng 492 nm. Một đối chứng kháng thể đơn dòng gồm kháng nguyên, kháng thể đơn dòng và enzym conjugate khi không có mặt huyết thanh của mẫu được thực hiện trên mỗi vỉ và được dùng để tính toán tỷ lệ cản trở đối với mỗi serum (PI: Percentage Inhibition). Nếu huyết thanh của mẫu cho giá trị PI > 50% (50% giảm mật độ màu), được coi là dương tính .
Thử nghiệm này đã thay thế phần lớn phản ứng ELISA gián tiếp và phản ứng trung hòa virus trong việc kiểm tra huyết thanh sau khi tổ chức tiêm phòng dịch tả trâu bò.
7.4.Chẩn đoán phân biệt:
Trên trâu bò, không thể phân biệt bệnh dịch tả trâu bò với bệnh BVD (bovine viral diarrhoea). Ơ cừu và dê, bệnh dịch tả dê cừu (PPR: peste des petits ruminants) cũng giống hệt bệnh dịch tả trâu bò. Đặc biệt bệnh thể nhẹ chỉ có tiêu chảy thì khó phân biệt với các bệnh đường ruột khác.
8. kiểm soát bệnh:
Bệnh dịch tả trâu bò lan tràn khá chậm ở các nước có dịch (endemic), chủ yếu gây bệnh ở thú non. Biện pháp kiểm soát bệnh là tiêm phòng hàng năm cho tất cả thú non. Những nước muốn loại trừ bệnh dịch tả trâu bò thì cần tiêm phòng cho toàn bộ trâu, bò, dê, cừu trong vòng 3-5 năm. Ơ các nước kế bên các vùng có dịch hoặc khi nhập khẩu thú từ các vùng có dịch thì cần phối hợp kiểm dịch và tiêm phòng.
Vaccine:
Các thú mẫn cảm có thể được gây miễn dịch tốt nhờ vaccin sống giảm độc. Ơ nhiều giai đoạn khác nhau, virus đã được giảm độc trên thỏ, dê, và tế bào nuôi cấy. Miễn dịch tạo ra thường kéo dài một thời gian lâu. Vaccin dịch tả trâu bò nuôi cấy tế bào (TCRV) đã được sản xuất ở Đông Phi châu với sự giảm độc của dòng virus cường độc Kabete “O”. Nó có nhiều ưu điểm hơn loại thỏ hóa hoặc dê hóa và là loại vaccin dịch tả trâu bò duy nhất được OIE chỉ định. Nó cũng được dùng phòng bệnh ở sở thú và trên trâu, bò, dê, cừu.
Tiêu chuẩn giống vaccin:
a-Đặc điểm:
Các chủng dùng phải có nguồn gốc rõ ràng và qua quá trình giảm độc được nuôi cấy trên tế bào cho thấy an toàn và tạo miễn dịch ít ra 5 năm trên trâu bò. Ngoài ra nó phải chứng tỏ không trở lại tính cường độc khi tiêm truyền ít ra 5 đời liên tiếp trên trâu bò (bản động vật ) cũng như không làm lây lan bịnh. Hiện chỉ có chủng Kabete O (RBOK: rinderpest bovine old kabete) là đạt các yêu cầu trên.
b-Nuôi cấy:
Chủng vaccin được hình thành sau 90-120 đời cấy truyền, được bảo quản ở nhiệt độ thấp hơn – 20oC và trong tình trạng đông khô. Virus thường được nuôi trên tế bào thận của phôi bê hoặc bê rất non. Tế bào thận không nên dùng nhân quá 10 đời kể từ dòng đầu tiên.
c-Tính ổn định của chủng làm vaccin:
- Thuần khiết, không có nhiễm virus khác hoặc nhiễm vi khuẩn, nấm hay Mycoplasma.
- An toàn, không gây ảnh hưởng bất thường trên thú mẫn cảm.
- Hiệu qua, gây miễn dịch tốt trên thú mẫn cảm.
Sản xuất vaccin:
Các lô vaccin riêng biệt được điều chế bằng cách gây nhiễm tế bào nuôi cấy và sau thời gian nuôi cấy thích hợp, thu hoạch lớp môi trường bên trên vì chúng chứa một số lớn virus giải phóng ra. Để bảo quản được lâu và phân phối, dịch trên được trộn thêm chất bảo quản gồm 5% lactalbumin, 10% sucrose rồi cho đông khô. Virus có thể phát triển trên tế bào thận sơ cấp từ bê hoặc phôi bê.
Kiểm tra trong quá trình sản xuất:
Kiểm tra tế bào: Các tế bào sơ cấp hoặc thứ cấp phải lấy từ các bê hoặc phôi bê có vẻ khỏe mạnh và phải giữ hình dạng bình thường trong khi nuôi cấy và không bị nhiễm các virus khác như virus gây tiêu chảy bò (BVDV). Trong khi sản xuất vaccin thì các môi trường đối chứng không cấy virus phải giữ ở cùng một điều kiện như các tế bào đang nuôi cấy virus. Thường xuyên phải kiểm tra qua kính hiển vi. Sau khi thu hoạch virus, môi trường đối chứng được rửa để lấy đi huyết thanh bò đực (ox serum) và thế vào đó huyết thanh bò đực mới và được ủ tiếp 10 ngày. Chúng phải được kiểm tra thường xuyên qua kính hiển vi để phát hiện bất cứ biến đổi bệnh tích tế bào nào. Đồng thời, cũng phải kiểm tra các virus BVD có thể nhiễm vào tế bào nuôi cấy không gây bệnh tích tế bào bằng kỹ thuật miễn dịch huỳnh quang hoặc IP (immuno-peroxidase). Các thành phần huyết thanh dùng nuôi tế bào phải được chứng tỏ không có các tác nhân gây trung hòa virus trước khi được sử dụng.
Kiểm tra virus: Định lượng virus phải thực hiện với giống vaccin bằng cách pha loãng theo cơ số 10 (10, 100, 1000, ...) trong 1 vỉ nhỏ hoặc hệ thống ống nghiệm xoay tròn, mỗi nồng độ cần 10 lỗ. Cũng cần định lượng tương tự đối với thành phẩm. Virus không nên nuôi quá 10 ngày. Dịch chứa virus thu được cho ly tâm với tốc độ thấp để loại cặn (làm trong) trước khi trộn với chất bảo quản làm lạnh. Nó phải được giữ không quá 5 ngày ở 4 độ C nhưng có thể lâu nếu đông lạnh ở -20 độ C đến -60 độ C . Thành phẩm phải thử nghiệm không nhiễm vi khuẩn, nấm và Mycoplasma.
Kiểm nghiệm vaccin (Batch control):
Mẫu phải được lấy cho mỗi đợt sản xuất, được kiểm tra các chỉ tiêu sau đây:
- Vô trùng (sterility),
- An toàn.
Vaccin lấy từ 5 lọ (lấy ngẫu nhiên) được trộn lại và dùng để chích vào 1 bò đực mẫn cảm với số lượng 100 liều tiêm và 1 con với 1/10 liều tiêm thông thường. Các thú này được nhốt chung với 1 con bò đực chưa tiêm phòng trong vòng 3 tuần lễ. Hàng ngày phải đo thân nhiệt và theo dõi triệu chứng lâm sàng. Sau giai đoạn này, con vật được kiểm tra kháng thể bằng phản ứng trung hòa và công thử thách với 1 chủng virus dịch tả trâu bò có thể gây sốt. Vaccin được coi như an toàn và hiệu quả nếu nó không gây triệu chứng nào bất thường, nếu cả 2 thú được chủng vaccin đều được bảo hộ và không thấy có sự truyền lây virus. Mỗi một lô vaccin phải được thử tính không gây bệnh trên tiểu gia súc.
- Khả năng gây miễn dịch:
Quan hệ chặc chẽ giữa khả năng gây miễn dịch và tính xâm nhiễm tế bào cho thấy có thể dùng cái sau để đánh giá cái trước. 3 thử nghiệm gây bệnh trên tế bào dùng loại tế bào nuôi cấy có nguồn gốc từ 3 thận bê hoặc thận phôi bê khác nhau. Trường hợp đầu tiên dùng đánh giá tính an toàn, trường hợp thứ 2 và thứ 3 được dùng để ước lượng, mỗi cái được lấy từ 3 container thành phẩm. Tính nhạy cảm của tế bào dùng sản xuất phải được đo lường bằng cách dùng các chế phẩm chuẩn hóa. Chuẩn độ sau cùng là trung bình hình học MG của 3 ước lượng trên, mỗi cái dùng hệ thống pha loãng 1:10 và 10 lặp lại ở mỗi nồng độ pha loãng.
- Độ dài miễn dịch:
Các kết quả cho thấy miễn dịch kéo dài sau khi tiêm vaccin cho trâu bò đã hết ảnh hưởng của miễn dịch từ mẹ (qua sữa đầu).
- Tính ổn định:
Vaccin rất ổn định trong trạng thái đông khô và có thể bảo quản trên 4 năm ở nhiệt độ 4 độ C hoặc -10 độ C nếu giữ cẩn thận. Các mẫu đại diện có thể được kiểm tra xem độ ẩm còn lại và tính ổn định ở 37 dộ C. Sau khi phục hồi, huyễn dịch virus rất mau thoái hóa nên thời gian sử dụng trong hiện trường không được quá 1 ngày làm việc.
Receive articles via Email!